我们生活的物质世界,小到尘埃、大到星球,皆由原子构成。单个原子孤立存在时极不稳定,它们总会通过某种作用力相互结合,形成分子、晶体等稳定结构。这种将原子紧密连接在一起的“无形纽带”,就是化学键,它是原子间强烈相互作用的统称,也是物质保持稳定形态的核心原因。
化学键的本质是原子间的电性相互作用,根据成键方式的不同,主要分为共价键、离子键和金属键三大类,它们如同三种不同的“连接方式”,让原子们各展所长,构成多样物质。
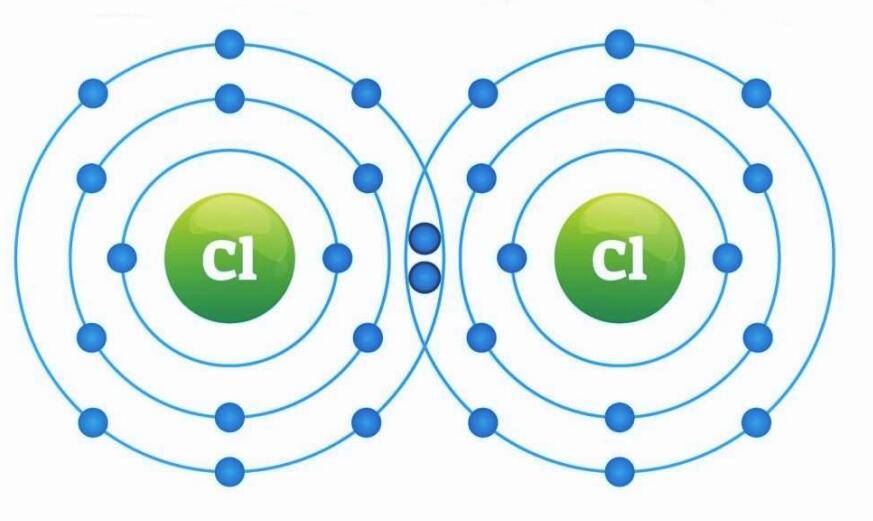
共价键是最常见的结合方式,多存在于非金属原子之间。当两个电负性相近的原子相遇时,它们不会轻易失去或得到电子,而是通过共用电子对达成稳定结构,就像两个伙伴共享玩具一样。例如氢原子和氧原子结合成水分子时,每个氢原子拿出1个电子,氧原子拿出2个电子,形成两对共用电子对,将三个原子牢牢结合。共价键具有饱和性和方向性,一个原子能形成的共价键数目是固定的,且原子轨道会沿特定方向重叠,这也决定了分子的空间结构。
离子键则是活泼金属与活泼非金属原子之间的“纽带”。电负性差异较大的两类原子相遇时,金属原子会失去最外层电子形成阳离子,非金属原子会得到电子形成阴离子,正负离子通过静电作用相互吸引,最终达到平衡形成离子键。比如氯化钠的形成,钠原子失去1个电子变成钠离子,氯原子得到1个电子变成氯离子,两者通过静电引力结合成稳定的离子晶体。离子键无方向性和饱和性,离子会在空间中尽可能多地吸引异号离子,形成规整的晶体结构。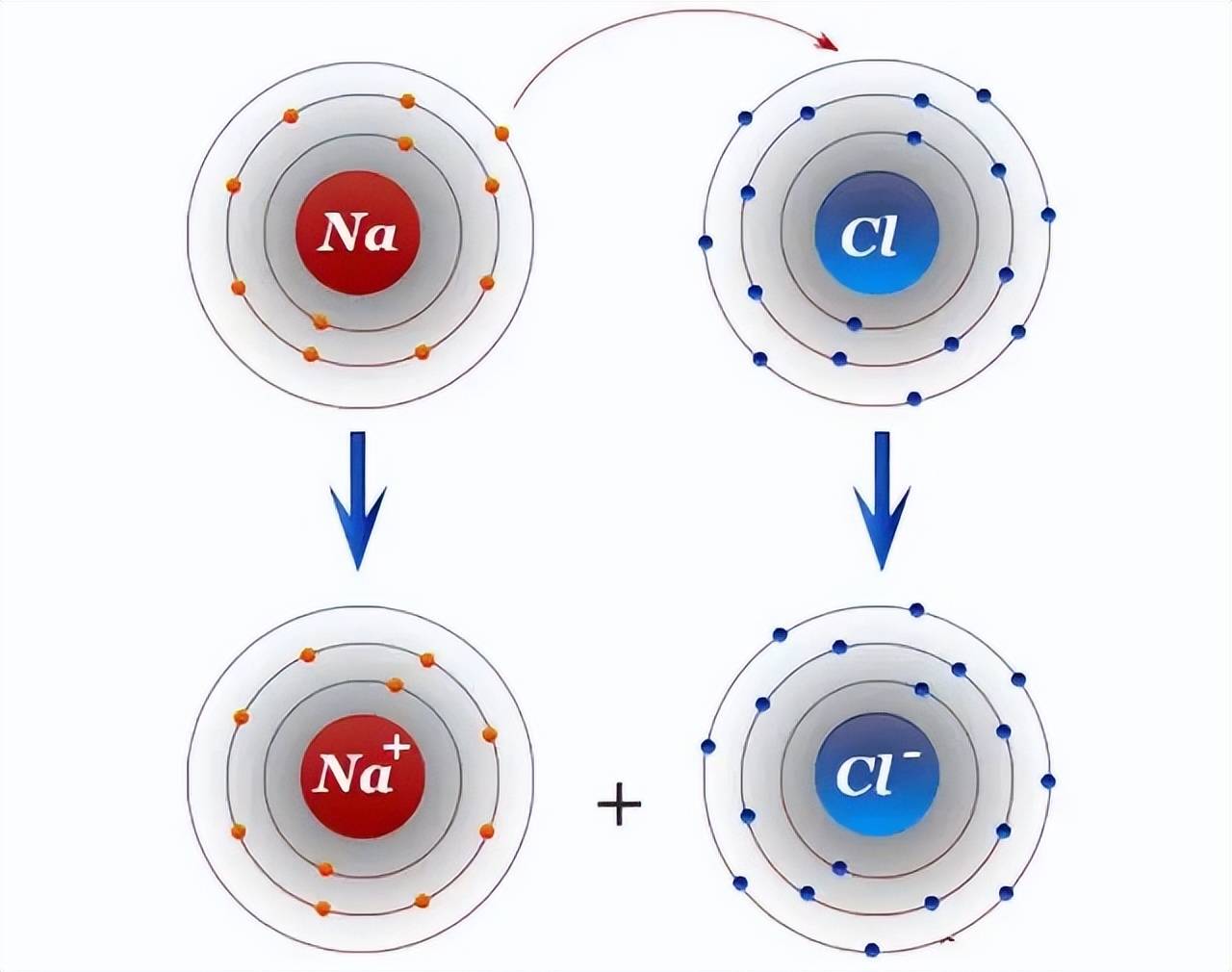
金属键是金属单质中原子结合的关键。金属原子的电离能低,容易失去价电子,这些电子脱离原子后成为自由电子,在金属阳离子之间自由流动,如同“电子海”。自由电子与金属阳离子之间的静电吸引力,就形成了金属键。这种成键方式让金属具有良好的导电性、导热性和延展性,比如铜能导电,就是因为自由电子可以在电场作用下定向移动。
值得注意的是,这三种化学键并非绝对独立,很多化合物中会存在化学键的过渡形态,不存在纯粹的离子键或共价键。化学键的理论也在不断发展,从经典价键理论到现代分子轨道理论,科学家们逐步揭开了原子结合的本质。
正是这些看不见的化学键,将无数原子有序结合,构成了我们身边的万事万物。从空气中的氧气、水中的水分子,到我们使用的金属制品,化学键始终发挥着核心作用,它不仅是化学世界的基础,更是连接微观原子与宏观物质的桥梁。